注册与销售第二类医疗器械公司的关键知识与步骤

注册并销售第二类医疗器械是一项专业性强、法规要求严格的企业活动,涉及医疗、法律、商业和质量管理等多领域知识。以下是需要掌握的核心知识和步骤:
一、法规基础与分类认知
- 医疗器械分类管理:中国对医疗器械实行分类管理,第二类医疗器械是具有中度风险,需要严格控制管理以保证其安全、有效的器械,如血压计、体温计、医用缝合针等。必须准确界定产品类别,依据《医疗器械分类目录》。
- 核心法规:熟悉《医疗器械监督管理条例》、《医疗器械经营监督管理办法》等国家法规,以及地方药品监督管理局的具体要求,这是合规经营的根本。
二、公司注册与许可流程
- 公司注册:首先完成工商注册,确定公司名称、注册资本(通常无特殊要求,但需满足运营需求)、经营范围(需明确包含“第二类医疗器械销售”)。
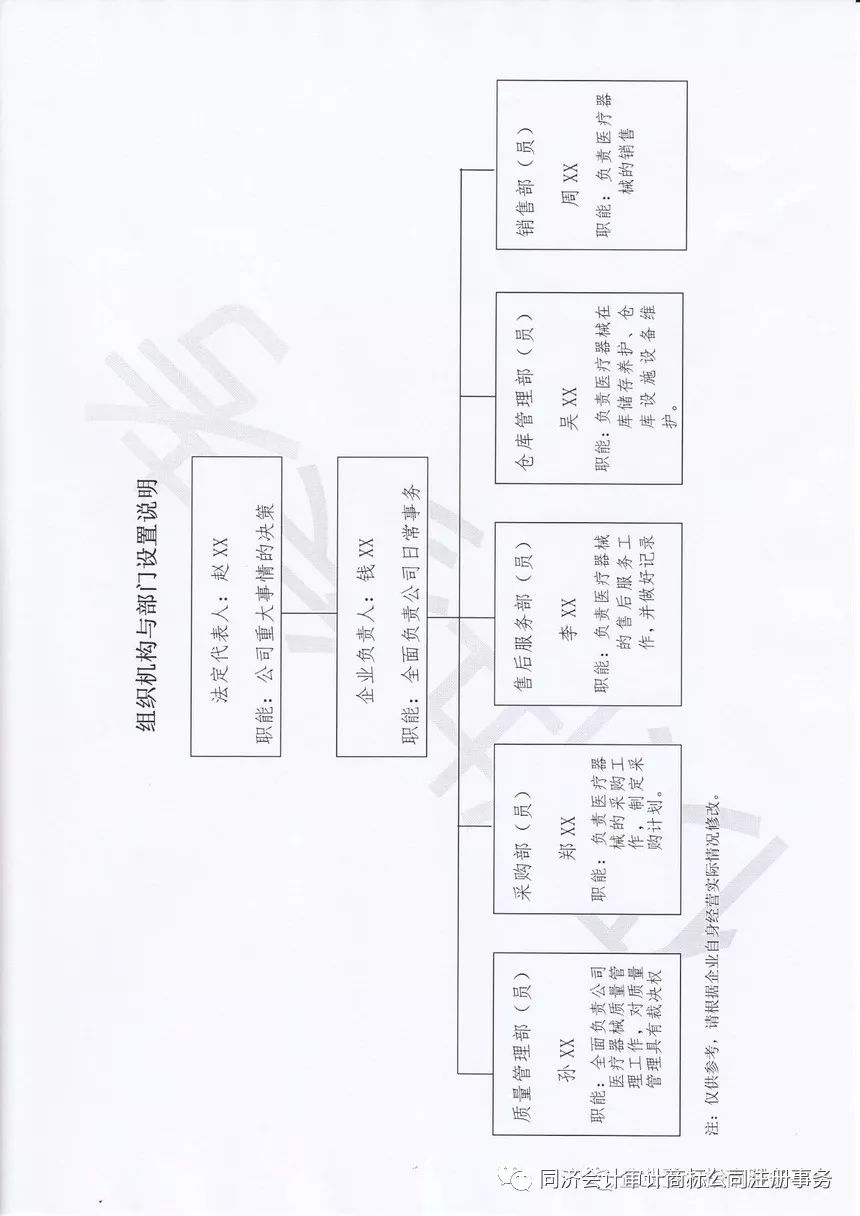
- 经营备案或许可:销售第二类医疗器械实行备案管理。向所在地设区的市级药品监督管理部门提交备案材料,获得《第二类医疗器械经营备案凭证》后方可经营。备案材料通常包括:营业执照复印件、法定代表人、企业负责人、质量负责人的身份证明与学历或职称证明(质量负责人需具备相关专业背景或工作经验)、组织机构与部门设置说明、经营场所和库房的地理位置图及房屋产权或租赁协议、经营设施设备目录、经营质量管理制度与工作程序文件目录等。
- 人员要求:企业负责人应熟悉医疗器械法规,质量负责人需具备医疗器械相关专业(如医学、药学、生物工程等)大专以上学历或中级以上职称,并具有3年以上医疗器械经营质量管理工作经历。
三、质量管理体系建立
- 制度文件:建立覆盖采购、验收、贮存、销售、运输、售后服务等全过程的质量管理制度,如质量职责、采购控制、记录管理、不合格品处理、不良事件监测和报告等制度。
- 设施与仓储:具有与经营规模和经营范围相适应的经营场所和库房。库房要求环境整洁、无污染源,具有符合医疗器械贮存要求的设施设备(如温湿度监测与调控设备、避光通风设施等)。经营场所与库房应独立设置,面积需满足经营需求。
- 记录与追溯:严格执行进货查验和销售记录制度,确保产品可追溯。记录应真实、完整、准确,保存期限不得少于医疗器械有效期后2年,无有效期的不少于5年。
四、销售运营与合规要点
- 供应商与产品资质审核:采购前必须审核生产厂家或供应商的《医疗器械生产许可证》或《医疗器械经营许可证》/备案凭证,以及产品的《医疗器械注册证》或备案凭证,确保来源合法。
- 销售管理:不得销售未注册/备案、无合格证明、过期、淘汰的医疗器械。向使用单位销售时,应核实其资质。销售记录应包含产品名称、规格、批号、有效期、购销单位等信息。
- 广告与宣传:医疗器械广告需经审查批准,内容必须真实、合法、科学,不得夸大功效。
- 不良事件监测与报告:建立不良事件监测制度,发现可疑不良事件应按要求向监测机构报告。
五、持续合规与法律责任
- 监督检查:药监部门会进行日常监督检查、飞行检查等,企业需保持体系持续运行并配合检查。
- 变更与延续:备案信息发生变更(如地址、质量负责人)需及时办理变更备案。《备案凭证》长期有效,但企业需持续符合条件。
- 法律责任:违规经营将面临警告、罚款、责令停业、吊销备案凭证直至追究刑事责任等处罚。
成功注册并运营一家第二类医疗器械销售公司,关键在于深入理解法规、建立健全的质量管理体系、确保全程合规操作,并将安全有效置于商业利益之上。建议在筹备阶段咨询专业法律或咨询机构,并与当地药监部门保持良好沟通。
如若转载,请注明出处:http://www.tbsaasmall.com/product/33.html
更新时间:2026-05-29 08:50:05